Top
Top熱意と挑戦の開発プロジェクト
駆け抜けた30年の軌跡
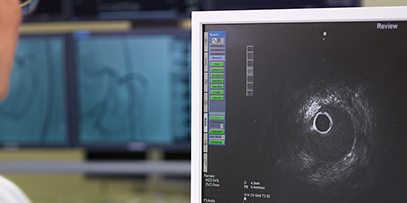
心臓移植は、心臓病が悪化し、心臓の機能が損なわれた重症心不全の患者さんの治療の最後の選択肢ですが、移植を必要としながらもドナーが見つかるのを待っている患者さんが数多くいます。植込み型左心補助人工心臓システムは、移植までの間、患者さんの心臓の補助をして生命を支える医療機器です。テルモは、患者さんの身体的負担を少しでも減らすことを目指すとともに、その人らしい日常生活を送れるようにという信念を胸に、試行錯誤を重ね製品開発を行ってきました。
このテルモの植込み型左心補助人工心臓の開発プロジェクトは、すでに新製品の開発を終了し、現在は製品を使用中の患者さんのサポートのみを残し、約30年にわたる歴史に終止符を打とうとしています。
しかしながら、植込み型左心補助人工心臓はテルモにとって大きな意味をもつ製品です。開発の過程で得た新しい技術や知見が、その後の研究開発に継承されていることも重要ですが、それに留まらず、テルモの企業理念「医療を通じて社会に貢献する」を、テルモのアソシエイト(社員)たちが最も強く実感することとなった製品の一つと言っても過言ではありません。今回はその歴史を振り返ります。
重症心不全の患者さんを救うため
進化し続けた人工心臓
重症心不全の患者さんの治療に用いられる人工心臓の開発は1930年代に始まり、当時は、実際の心臓の模倣を目指していました。心臓を取り出し、心機能そのものを装置に置き換える治療法でしたが、初期の人工心臓は耐久性がなく、血栓の発生や感染症のリスクに晒され、また、装置が大型なため、装着した患者さんは寝たきり状態になってしまうなど、多くの課題を抱えていました。
なかなか実用化には至らなかった人工心臓の開発は、1969年に転換期を迎えます。これまでの「心臓を置き換える」という考えから、心臓を移植するまでの「つなぎ(ブリッジ)に使う」という新しい発想が生まれ、人工心臓の役割は大きく変化しました。さらに、患者さんの心機能で、最も負担が大きく、弱りやすいのが左心室であったことから、左心室の働きを助け、心機能の回復を促す「左心補助人工心臓」が開発の主流となっていったのです。1981年、心臓外科医の阿久津博士がつくり上げた人工心臓が、心臓移植までの「つなぎ」として実際に使用されたことで本格的な臨床の時代へと進んでいきます。
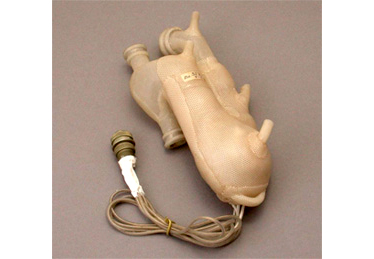
阿久津博士が製作した初期の
人工心臓全置換型人工心臓
(TAH: total artificial heart)
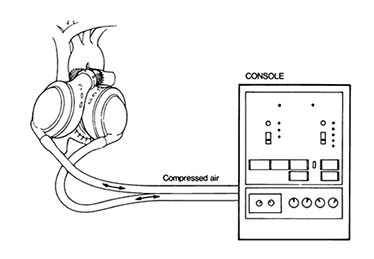
アクツ・モデルⅢ型
(Division of Surgery:Texas Heart Institute, 8(3),
305-319,1981より)
テルモにおける人工心臓開発は、1983年に北海道大学と共同でポンプの開発を試みたことに始まります。しかし、技術的な課題により一旦中断しました。1989年、当時のテルモの社長である戸澤の招きにより、この人工心臓開発の第一人者である阿久津博士がテルモの人工心臓開発の最高責任者兼副社長に就任。さらに、1991年には、東京女子医科大学の心臓外科医だった野尻知里博士を研究開発センター客員研究員として招き、テルモでも補助人工心臓の開発が本格的に再始動したのです。
血液へのやさしさを追求
第三世代「磁気浮上型遠心ポンプ」の誕生
人工心臓の血液を送り出すポンプは、生きた心臓と同じように脈を打つ第一世代「拍動流ポンプ」から、水道の水のように一定の流れで血液を流す第二世代「連続流ポンプ」へと開発が進んでいました。この第二世代ポンプを使った装置は、小型化や軽量化が可能になり、初期の人工心臓に比べて患者さんの負担を格段に軽減することができました。しかし、血液を送り出す羽根車を回転させる軸と、その軸受け部分で摩擦が起こり、回転に不具合が生じたり、血液が異物にふれ血栓ができたりと問題がありました。
テルモは、補助人工心臓の開発にあたり、最大の課題である「血栓の発生をいかに防ぐか」を解決するために、1994年に京都大学とベアリングメーカーNTN社が考案した「磁気浮上型遠心ポンプ」という技術の導入を決め、共同開発を開始。この技術は、磁力を利用して羽根車を浮かせたまま回転させるというもので、この技術により血液室内での機械摩擦をなくすことができれば、血栓の発生リスクを低減できると考えました。このポンプ技術を用いた補助人工心臓は、1997年に行われた動物実験で864日間という世界最長(当時)となる連続運転を記録し、この技術を用いればポンプが長期間使用可能であることが確認できました。加えて、本体をチタン製に改良し、1998年には植込み型左心補助人工心臓として商品化することが決まったのです。
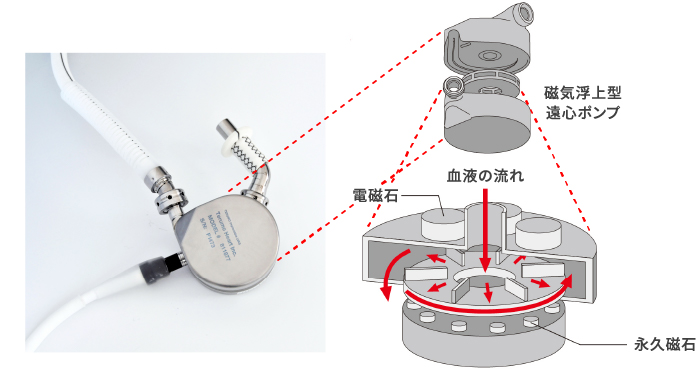
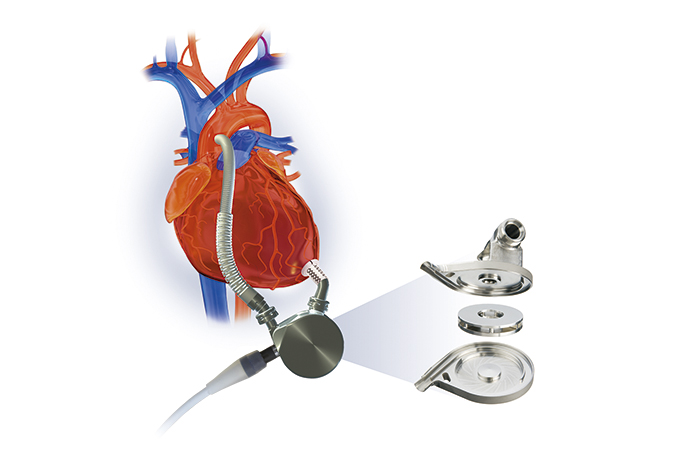
磁気浮上型遠心ポンプの構造
販売後の技術的課題を克服するも
厳しい市場状況の中、プロジェクト終焉へ
当時、テルモでは人体に影響を与えるリスクが最も高い、クラスⅣの医療機器の商品化経験はなく、日本では、開発環境も整っていませんでした。一方、米国では、国策として医療を産業の柱とし医療機器の開発を進めていたことから、開発に必要な技術や人材などの環境が整っていました。その状況下から、テルモでは、患者さんのためにいち早く実用化を進めるために、2000年に開発拠点を米国へ移したのです。
その後、2004年1月に欧州で、続けて米国や日本でも、テルモの補助人工心臓の臨床試験を開始。さまざまな課題に直面しながら、臨床試験を続け、ついに2007年に欧州で、そして2011年に日本で、植込み型左心補助人工心臓システムの販売が開始されました。しかし、ポンプの通常の回転モード(磁気浮上方式)が維持されないという不具合が発生したことから、同年、国内での新規植込みを一時見合わせることになりました。
2013年7月、改良を重ね、国内で製品販売を再開しましたが、電子部品の調達や製品の供給、機器の保守を確実に対応できる期間にも物理的な限界があることから、2017年3月末をもって植込みに関連する製品の供給を終了することを関連施設に対してアナウンスしました。一方、欧米においても、競合他社との競争は厳しく、2012年には欧州での販売終了、米国での治験の中断を決めました。初代のものよりもさらに小型にした次世代機の開発も進んでいたものの、2013年にその技術を他社に売却し開発事業は終了を迎えます。
現在、植込み型左心補助人工心臓システムを装着した患者さんは2名(2021年3月現在)いらっしゃいます。テルモは、患者さんが製品を必要としなくなる日まで、これまでと同様にサポートを続けていきます。
補助人工心臓の開発の先陣を切り、
医療の質向上に貢献
植込み型補助人工心臓をとりまく状況は、ここ10年で大きく変化しています。日本では、当初5施設しかなかった、補助人工心臓を植え込むことができる施設は、現在では46施設にも増えています。また、使える機種は海外の機種を含め5機種まで増え、当時は特別だった補助人工心臓による治療も、徐々に一般的な治療になってきています。テルモの製品開発は終わりを迎えたものの、開発を通して、医療技術の向上や治療法の普及に貢献できたと考えています。
また、開発の過程でチームが残したさまざまな技術は、以後の製品へと引き継がれています。そして、開発の支柱であった野尻氏は、2015年11月13日に永眠されましたが、その存在は大きく、「困っている患者さんを助けたい」という志は、プロジェクトチームの皆が同じ想いを共有していました。この信念のもと、30年にもわたった一大プロジェクトは、当時のテルモのビジョンであった「ユニークで輝く技術で、人にやさしい医療を実現する」を体現していました。開発に没頭した年月は、かけがえのない大きな財産になり、また、その経験と強い信念は、テルモのDNAとして受け継がれています。