
News release
テルモのニュースリリースは、当社企業活動をステークホルダーの皆様にお伝えするためのものです。医療機器や医薬品の情報が含まれることがありますが、これらは報道関係者、株主・投資家等の皆様を対象にした情報であり、顧客誘引や医学的アドバイスを目的とするものではありません。
世界初となる心不全治療用の再生医療製品
 Top
Topテルモ株式会社(本社:東京都渋谷区、社長:新宅 祐太郎)は、再生医療等製品として申請していたヒト(自己)骨格筋由来細胞シート「ハートシート」が、本日、厚生労働省より条件及び期限付承認を取得しましたのでお知らせします。
ハートシートは、虚血性心疾患による重症心不全を対象とした患者さん向けの製品で、患者さんの大腿部より筋肉組織を採取し、組織内に含まれる骨格筋芽細胞を培養してシート状にします。シートを患者さんの心臓表面に移植することで、重症心不全の病態改善が期待できます。培養する細胞は患者さん自身から採取する自家細胞のため、拒絶反応がないことが特徴として挙げられます。
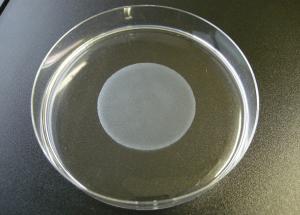
「本品により調製されたシート」(シャーレ中央)
今回の条件及び期限付承認では、①60例における治療の有効性に関する情報、②既存治療を行う群(120例)との比較で生存率における優位性の確認、③5年以内に承認申請を行うことが条件となりました。

テルモ施設における細胞培養の様子
参考1:テルモは、心筋再生医療について、2007年より細胞シートの開発に着手し、2012年から国内3医療機関で7例の治験を実施し、2014年に完了いたしました。その後、2014年10月30日、厚生労働省へ再生医療等製品として、ハートシートの製造販売承認申請を行っていました。
参考2: ハートシートは、NEDO※のプロジェクトで大阪大学大学院医学系研究科 心臓血管外科 澤芳樹教授が開発を進め、臨床研究が実施されてきました。当社は、大阪大学との共同研究を進め、先端医療開発特区「スーパー特区」の「細胞シートによる再生医療実現プロジェクト」(研究代表者:東京女子医科大学岡野光夫教授)に参加しました。※国立研究開発法人新エネルギー・産業技術総合開発機構
【ハートシート効能又は効果について】
下記の基準をすべて満たす、薬物治療や侵襲的治療を含む標準治療で効果不十分な虚血性心疾患による重症心不全の治療
<対象とする心不全の状態>・NYHA心機能分類がⅢ又はⅣ度、・安静時における左室駆出率が35%以下
テルモは、「医療を通じて社会に貢献する」という理念を掲げ、100年の歴史を持つ医療機器メーカーです。日本に本社を構え、世界160以上の国と地域で事業を展開、30,000人以上のアソシエイト(社員)が革新的なソリューションを届けるために日々働いています。
国産体温計の製造に始まり、設立以来、医療の基盤を支え続けてきました。現在は、カテーテル治療、心臓外科手術、薬剤投与、糖尿病管理、腹膜透析、輸血や細胞治療などに関する幅広い製品・サービスを提供しています。
テルモは、患者さんや医療従事者をはじめ、広く社会にとって価値ある企業を目指します。