
News release
テルモのニュースリリースは、当社企業活動をステークホルダーの皆様にお伝えするためのものです。医療機器や医薬品の情報が含まれることがありますが、これらは報道関係者、株主・投資家等の皆様を対象にした情報であり、顧客誘引や医学的アドバイスを目的とするものではありません。
テルモ山口で製造するアダリムマブのバイオシミラーに関してGMP適合を取得
 Top
Top
テルモ株式会社(本社:東京都渋谷区、社長:佐藤 慎次郎)の100%子会社であるテルモ山口D&D株式会社(山口県山口市)は、製造を受託するバイオシミラーに関して、GMP (Good Manufacturing Practice) 適合を取得しました。
このたびのGMP適合の対象は、協和キリン富士フイルムバイオロジクス株式会社が6月29日に日本での製造販売承認を取得したバイオシミラー*1であるアダリムマブBS皮下注「FKB」*2(先発医薬品: アッヴィ社「ヒュミラ」)です。関節リウマチや尋常性乾癬などの自己免疫疾患の治療に用いられ、テルモが開発したプラスチック製の注射器「PLAJEX」に薬剤が充填されています。
GMPとは医薬品の製造管理と品質管理に関する基準です。各国の規制当局は、製造所に対して、その製造管理手法が適切な品質の医薬品を製造できる体制であるかを調査し、認定をします。医薬品が販売承認を取得する際に、製品の品質・安全性・有効性を証明するとともに、製造所がGMPに適合する必要があります。
テルモ山口D&Dは、医薬品と医療機器を組み合わせた製品を製造しています。バイオ医薬品に適した設備や無菌充填技術と、これまでの製造の実績をもとに、製薬企業との提携ビジネスを展開しています。製剤設計や量産技術を共同開発し、患者さんに製品をいち早く届けることを目指しています。
テルモは引き続き、製薬企業のニーズに応える開発製造受託(CDMO)ビジネスを拡大し、より良い医療の普及に努めてまいります。
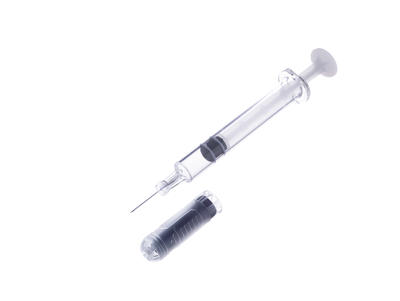
薬剤充填用の注射器PLAJEX

テルモ山口D&D
バイオシミラー(バイオ後続品)とは、既に承認されたバイオ医薬品と同等・同質の品質、安全性および有効性が認められた製品です。バイオ医薬品の有効成分は分子量が大きく構造が複雑なため、バイオシミラーの開発においては同等性・同質性を示すために新薬と同様に多くの試験が行われます。
製品の正式名称は、アダリムマブBS皮下注40mgシリンジ0.8 mL「FKB」、アダリムマブBS皮下注40mgペン0.8 mL「FKB」、アダリムマブBS皮下注20mgシリンジ0.4 mL「FKB」です。
テルモのテクノロジー「#03 患者さんに必要な薬を安全・確実に届ける技術」
https://www.terumo.co.jp/technology/stories/03/
テルモは、「医療を通じて社会に貢献する」という理念を掲げ、100年の歴史を持つ医療機器メーカーです。日本に本社を構え、世界160以上の国と地域で事業を展開、30,000人以上のアソシエイト(社員)が革新的なソリューションを届けるために日々働いています。
国産体温計の製造に始まり、設立以来、医療の基盤を支え続けてきました。現在は、カテーテル治療、心臓外科手術、薬剤投与、糖尿病管理、腹膜透析、輸血や細胞治療などに関する幅広い製品・サービスを提供しています。
テルモは、患者さんや医療従事者をはじめ、広く社会にとって価値ある企業を目指します。