ヒト(自己)骨格筋由来細胞シート

世界初※となる心不全治療用の再生医療製品。
虚血性心疾患による重症心不全を対象。*
自家細胞から製造した本品をシート状に調製し、心臓表面に移植。
*
【ハートシートの効能、効果又は性能】
下記の基準のすべてを満たす、薬物治療や侵襲的治療を含む標準治療で
効果不十分な虚血性心疾患による重症心不全の治療
<対象とする心不全の状態>
・NYHA心機能分類がⅢ又はⅣ度・安静時における左室駆出率が35%以下
- 1 骨格筋由来細胞シート心表面移植術に関する施設基準
- (1)植込型補助人工心臓(非拍動流型)の実施施設として届出のある施設又は植込型補助人工心臓(非拍動流型)の実施施設として届出のある施設と連携可能な施設であること。
- (2)医薬品医療機器等法に基づく薬局等構造設備規則又は再生医療等の安全性の確保等に関する法律(平成25年法律第85号)に基づく細胞培養加工施設の構造設備に関する基準に則った設備を有すること。
- (3)循環器内科の経験を5年以上有する常勤医師及び心臓血管外科の経験を5年以上有する常勤医師がそれぞれ1名以上配置され、これらの医師は所定の研修を修了していること。
- (4)定期的に循環器内科の医師と心臓血管外科の医師が参加する、心臓移植を含む重症心不全患者の治療方針を決定するカンファレンスが開催されていること。
- (5) 関連学会の定める「ヒト(自己)骨格筋由来細胞シートの使用要件等の基準について(2017年修正版)」
 において定められた実施施設基準に準じていること。
において定められた実施施設基準に準じていること。
- 第72の1の2 骨格筋由来細胞シート心表面移植術
(特掲診療料の施設基準等及びその届出に関する手続きの取扱いについて)
平成30年3月5日(保医発0305第3号)
商品に関するお問合せ先:0120-12-8195
(平日9:00~17:45)
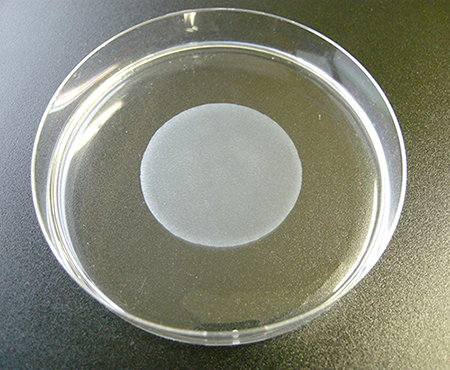
本品を使用して調製されたシート

 本品を使用して調製されたシート
本品を使用して調製されたシート
材料価格
- 189 ヒト骨格筋由来細胞シート
- (1)採取・継代培養キット:6,480,000円
- (2)回収・調製キット:1枚当たり1,710,000円
一般的名称:ヒト(自己)骨格筋由来細胞シート 販売名:ハートシート 製造販売承認番号:22700FZX00002000
製造販売業者:テルモ株式会社
〒151-0072 東京都渋谷区幡ヶ谷2-44-1
HeartSheet、ハートシートはテルモ株式会社の登録商標です。










